Mỗi liều 0,5 mL: các kháng nguyên bề mặt virus cúm (haemagglutinin và neuraminidase) các chủng* sau đây:
A/Victoria/2570/2019 (H1N1)pdm09-like strain (A/Victoria/2570/2019, IVR-215) 15 µg haemagglutinin/liều.
A/Cambodia/e0826360/2020 (H3N2)-like strain (A/Cambodia/e0826360/2020, IVR-224) 15 µg haemagglutinin/liều.
B/Washington/02/2019-like strain (B/Washington/02/2019, wild type) 15 µg haemagglutinin/liều.
B/Phuket/3073/2013-like strain (B/Phuket/3073/2013, wild type) 15 µg haemagglutinin/liều.
* đã nhân giống trong trứng gà mái được thụ tinh từ các đàn gà giò khỏe mạnh.
Vắc-xin này tuân theo khuyến cáo của Tổ chức Y tế Thế giới (Bắc bán cầu) và quyết định của nhà chức trách có thẩm quyền cho mùa 2021/2022.
Influvac 2021/2022 có thể chứa vết của trứng (như ovalbumin, protein gà), formaldehyde, cetyltrimethylamoni bromid, polysorbat 80 hoặc gentamicin, là những thành phần được sử dụng trong quá trình sản xuất (xem phần Chống chỉ định).
Danh mục tá dược
Kali clorid, kali dihydrogen phosphat, dinatri phosphat dihydrat, natri clorid, calci clorid dihydrat, magnesi clorid hexahydrat và nước cất pha tiêm.
Dạng bào chế
Hỗn dịch tiêm đóng sẵn trong các bơm tiêm, chất lỏng không màu, đóng liều đơn trong các bơm tiêm (thủy tinh, loại I).
Nhóm dược lý trị liệu: Vắc-xin cúm.
Mã ATC: J07BB02.
Cơ chế dược lý
Influvac tetra cung cấp hoạt tính miễn dịch cho bốn chủng virus: chủng A/(H1/N1), chủng A/(H3/N2) và hai chủng B (mỗi chủng từ một dòng B/(Victoria) và B/(Yamagata). Influvac tetra được sản xuất giống quy trình của vắc-xin cúm Influvac tam giá, gây ra kháng thể thể dịch kháng lại heamagglutinins. Những kháng thể này vô hiệu hóa virus cúm. Mức định lượng đặc hiệu kháng thể ức chế haemagglutinin sau khi tiêm với vaccine bất hoạt virus cúm không liên quan đến bảo vệ khỏi bệnh cúm nhưng định lượng kháng thể ức chế hemagglutination được dùng để đo hoạt động của vaccine. Đáp ứng miễn dịch đạt được trong 2-3 tuần. Khoảng thời gian miễn dịch đạt được sau khi tiêm với các chủng tương ứng hoặc đối với các chủng có quan hệ gần gũi với chủng của vaccine thay đổi nhưng thường trong 6-12 tháng.
Đặc tính dược lý
Miễn dịch của Influvac tetra so với Influvac tam giá
Nghiên cứu lâm sàng trên đối tượng người lớn trên 18 tuổi (INFQ3001) và trẻ em từ 3-17 tuổi (INFQ3002) đánh giá an toàn và miễn dịch của Influvac tetra và so sánh không kém hơn với Influvac tam giá cho định lượng hiệu giá kháng thể ức chế hemagglutinin trung bình sau khi tiêm (GMT)
Cả hai nghiên cứu đáp ứng miễn dịch từ Influvac tetra so với vaccine Influvac tam giá trong một nghiên cứu so sánh không kém hơn.
Người lớn hơn 18 tuổi và người già
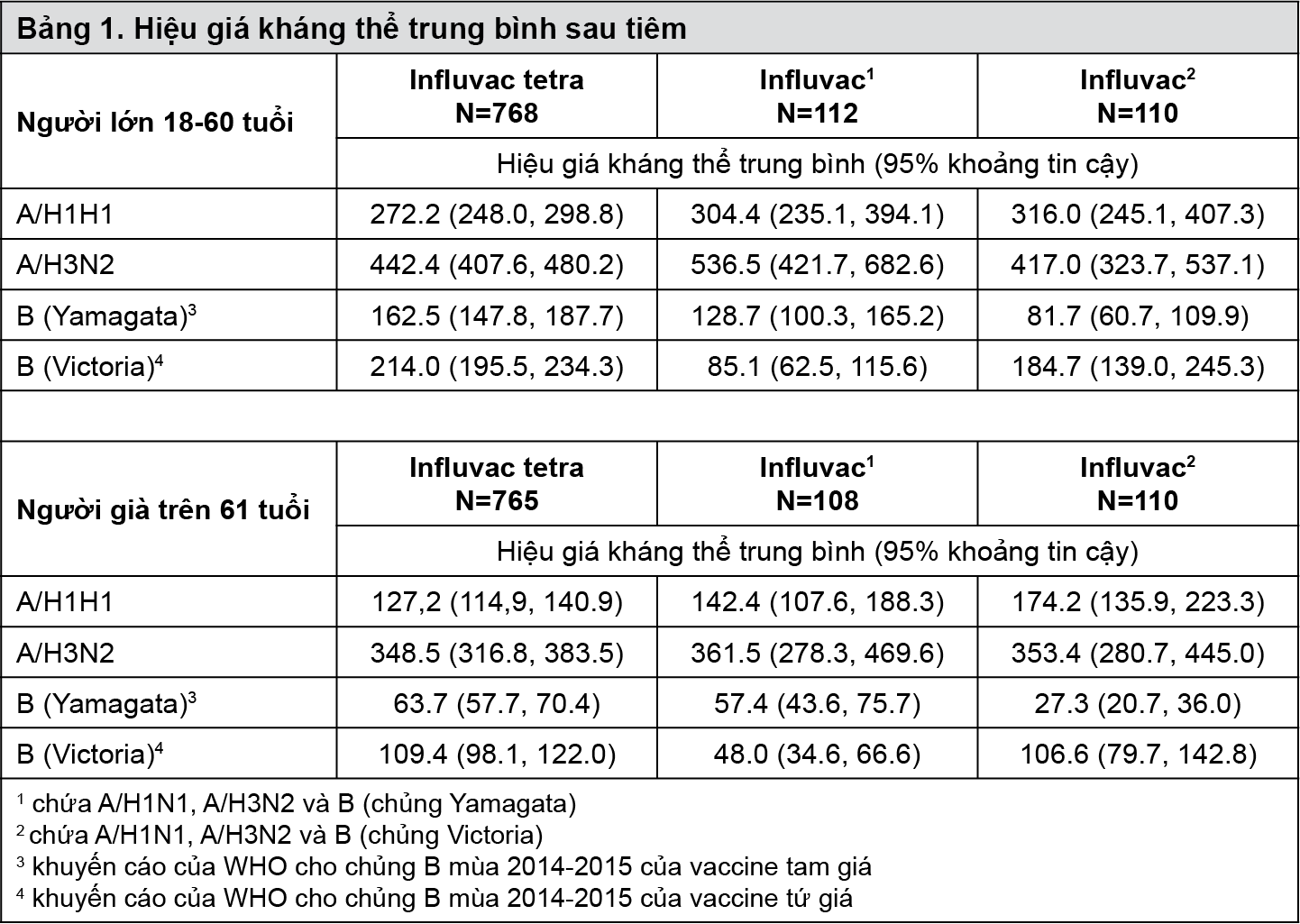
Nghiên cứu lâm sàng INFQ3001, 1535 người lớn trên 18 tuổi và người già nhận được liều đơn của Influvac tetra và 442 đối tượng nhận liều đơn Influvac tam giá.
- xem Bảng 1.
 Trẻ em
Trẻ em
Trẻ em từ 3-17 tuổi
Nghiên cứu lâm sàng INFQ3002, 402 trẻ em trong độ tuổi từ 3-17 được tiêm một hoặc hai liều Influvac tetra và 798 trẻ em được tiêm một hoặc hai liều Influvac tam giá dựa trên tiền sử tiêm vắc-xin cúm của trẻ.
- xem Bảng 2.
 Các số liệu an toàn tiền lâm sàng
Các số liệu an toàn tiền lâm sàng
Các dữ liệu tiền lâm sàng cho thấy không có nguy hại nào cho người dựa trên các nghiên cứu tiêu chuẩn về liều lặp lại và độc tính tại chỗ, cơ quan sinh sản và thử nghiệm độc tính và an toàn.
Phòng ngừa bệnh cúm, đặc biệt là ở những người có nguy cơ rủi ro tăng do biến chứng kết hợp.
Influvac tetra được chỉ định cho người lớn và trẻ em trên 3 tuổi.
Sử dụng Influvac tetra phải được dựa trên những khuyến cáo chính thức.
Liều lượng
Người lớn và trẻ em trên 3 tuổi: 0,5 mL.
Trẻ em dưới 9 tuổi, chưa tiêm vắc-xin cúm mùa, liều thứ 2 lặp lại nên được tiêm sau 4 tuần.
Đường dùng
Việc tiêm chủng nên được thực hiện bằng cách tiêm bắp hoặc tiêm sâu dưới da.
Cần cẩn trọng trước khi xử lý hoặc sử dụng sản phẩm.
Hướng dẫn về chuẩn bị sản phẩm trước khi dùng, xem phần Thận trọng lúc dùng - Các dấu hiệu cần lưu ý và khuyến cáo.
Mẫn cảm với các thành phần hoạt tính, với bất kỳ tá dược nào hoặc bất cứ thành phần nào có thể chỉ có mặt với một lượng rất nhỏ như trứng (ovalbumin, protein gà), formaldehyde, cetyltrimethylamoni bromide, polysorbat 80, hoặc gentamicin.
Các bệnh nhân/trẻ em có triệu chứng sốt hoặc nhiễm trùng cấp tính sẽ phải hoãn việc tiêm chủng.
Cũng như với tất cả các vắc-xin tiêm, điều trị nội khoa thích hợp và việc giám sát phải luôn luôn sẵn sàng trong trường hợp xảy ra phản ứng quá mẫn sau khi tiêm vắc-xin.
Không được tiêm tĩnh mạch Influvac tetra trong bất kỳ trường hợp nào.
Phản ứng lo âu, bao gồm cả phản ứng thần kinh phế vị (ngất), tăng thông khí hoặc phản ứng liên quan đến stress có thể xảy ra sau hoặc thậm chí trước khi tiêm chủng như là một phản ứng tâm lý. Điều này có thể được kèm theo một số dấu hiệu thần kinh như rối loạn thị giác thoáng qua, dị cảm và co giật chân tay khi vận động trong quá trình phục hồi. Quá trình tiêm chủng nên được thực hiện tại nơi có thể tránh bị chấn thương do ngất.
Đáp ứng kháng thể ở các bệnh nhân/trẻ em có ức chế miễn dịch nội sinh hoặc do điều trị có thể là không đủ.
Gây nhiễu các kết quả xét nghiệm huyết thanh học: xem Tương tác.
Thuốc chứa ít hơn 1 mmol natri (23 mg) trên 1 liều, tức là “không natri”.
Thuốc chứa ít hơn 1 mmol kali (39 mg) trên 1 liều, tức là “không natri”.
Ảnh hưởng của thuốc lên khả năng lái xe, vận hành máy móc
Influvac tetra không có hoặc có ảnh hưởng không đáng kể tới khả năng lái xe và vận hành máy móc.
Thời kỳ mang thai
Các vắc-xin cúm bất hoạt có thể được dùng trong tất cả các giai đoạn của thai kỳ. Dữ liệu về độ an toàn đối với thai kỳ thứ 2 và thứ 3 sẵn có hơn so với thai kỳ đầu tiên; tuy nhiên dữ liệu từ việc sử dụng rộng rãi vắc-xin cúm không cho thấy bất kì bất lợi trên phôi và người mẹ mang thai từ việc dùng vắc-xin.
Cho con bú
Influvac tetra có thể dùng được trong thời kỳ cho con bú.
Khả năng sinh sản
Không có dữ liệu về khả năng sinh sản.
Không có tương tác thuốc nào được thực hiện.
Nếu Influvac tetra được tiêm cùng một lúc với các vắc-xin khác, việc tiêm chủng phải được thực hiện trên các chi riêng biệt. Cần lưu ý rằng phản ứng bất lợi có thể tăng lên.
Đáp ứng miễn dịch có thể bị giảm nếu bệnh nhân đang điều trị ức chế miễn dịch.
Sau khi tiêm vắc-xin cúm, đã quan sát thấy các kết quả dương tính giả trong các xét nghiệm huyết thanh học sử dụng phương pháp ELISA để phát hiện các kháng thể chống lại HIV1, viêm gan C và đặc biệt là HTLV1. Kỹ thuật Western Blot bác bỏ các kết quả xét nghiệm ELISA dương tính giả. Các phản ứng dương tính giả nhất thời có thể là do đáp ứng IgM của vắc-xin.
Trong khi không có các nghiên cứu về tính tương thích, sản phẩm này không được trộn lẫn với bất kỳ dược phẩm nào khác.
a. Tổng quan về tính an toàn
Dữ liệu an toàn liên quan đến việc dùng Influvac tetra được dựa trên nghiên cứu lâm sàng ở người lớn mạnh khỏe trên 18 tuổi, trẻ em mạnh khỏe từ 3-17 tuổi được tiêm Influvac tetra hoặc Influvac tam giá. Trẻ em từ 3-8 tuổi được tiêm một hoặc hai liều Influvac tetra phụ thuộc vào tiền sử tiêm vắc-xin cúm của trẻ.
Hầu hết các phản ứng thường xảy ra trong 3 ngày đầu sau khi tiêm và tự động hết trong 1 đến 3 ngày bắt đầu. Cường độ của các phản ứng này nói chung là nhẹ.
Trong hầu hết các nhóm tuổi, tác dụng không mong muốn tại chỗ được báo cáo thường xuyên nhất sau khi tiêm chủng trong nghiên cứu lâm sàng của Influvac tetra là đau tại chỗ tiêm.
Các tác dụng không mong muốn toàn thân được báo cáo thường xuyên nhất sau khi tiêm chủng ở nghiên cứu lâm sàng Influvac tetra ở người lớn và trẻ em từ 6-17 tuổi là mệt mỏi và đau đầu, và ở trẻ từ 3-5 tuổi là buồn ngủ, khó chịu và chán ăn.
Tỷ lệ tác dụng không mong muốn tương tự đã được quan sát thấy ở những người tiêm Influvac tetra và Influvac tam giá.
b. Tóm tắt tổng hợp về tác dụng không mong muốn
Các tác dụng không mong muốn sau đây đã quan sát được trong thời gian thử lâm sàng của Influvac tetra đã được quan sát trong các nghiên cứu lâm sàng hoặc từ các nghiên cứu sau bán hàng của Influvac tam giá.
Tần số xuất hiện như sau:
Rất phổ biến (≥1/10); phổ biến (≥1/100, <1/10); không phổ biến (≥1/1000, <1/100); và không biết (các tác dụng không mong muốn sau bán hàng không dự đoán được từ các dữ liệu sẵn có).
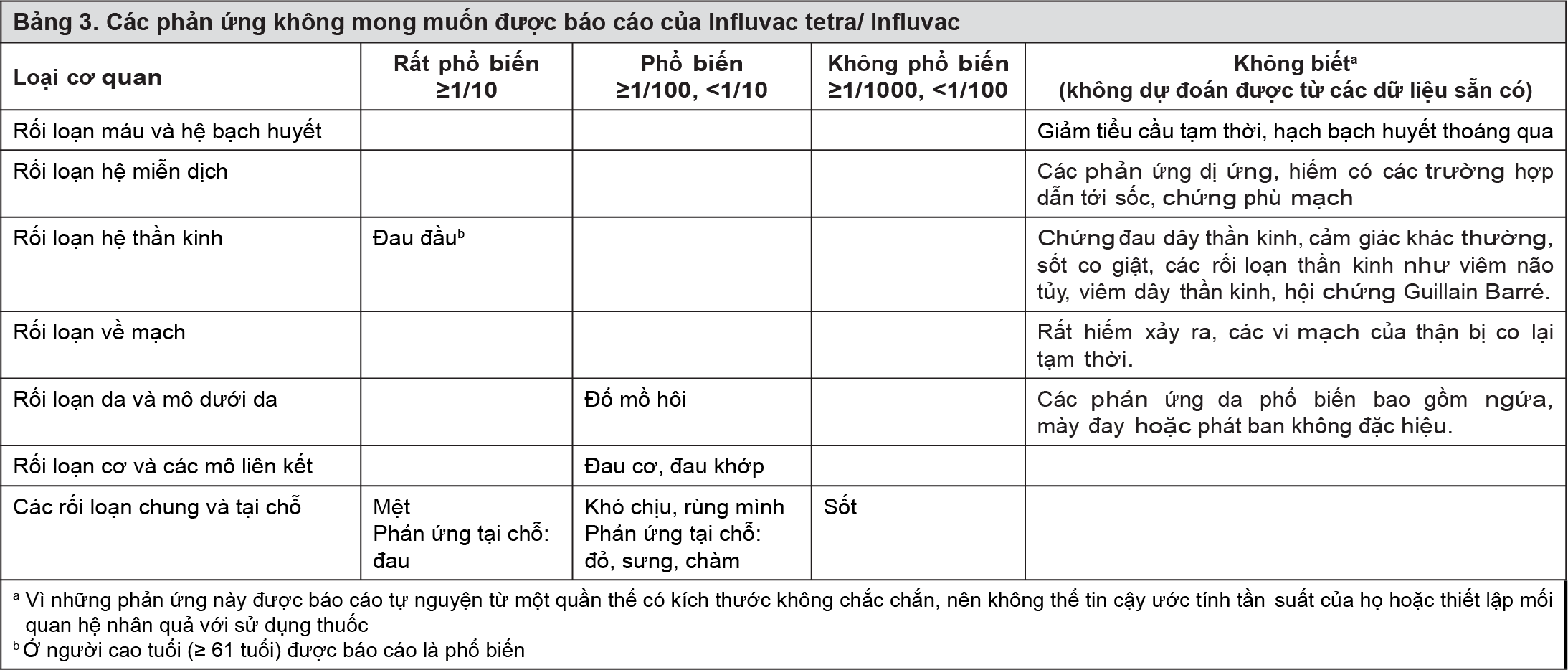
Người lớn và người lớn tuổi
- xem Bảng 3.
 Trẻ em
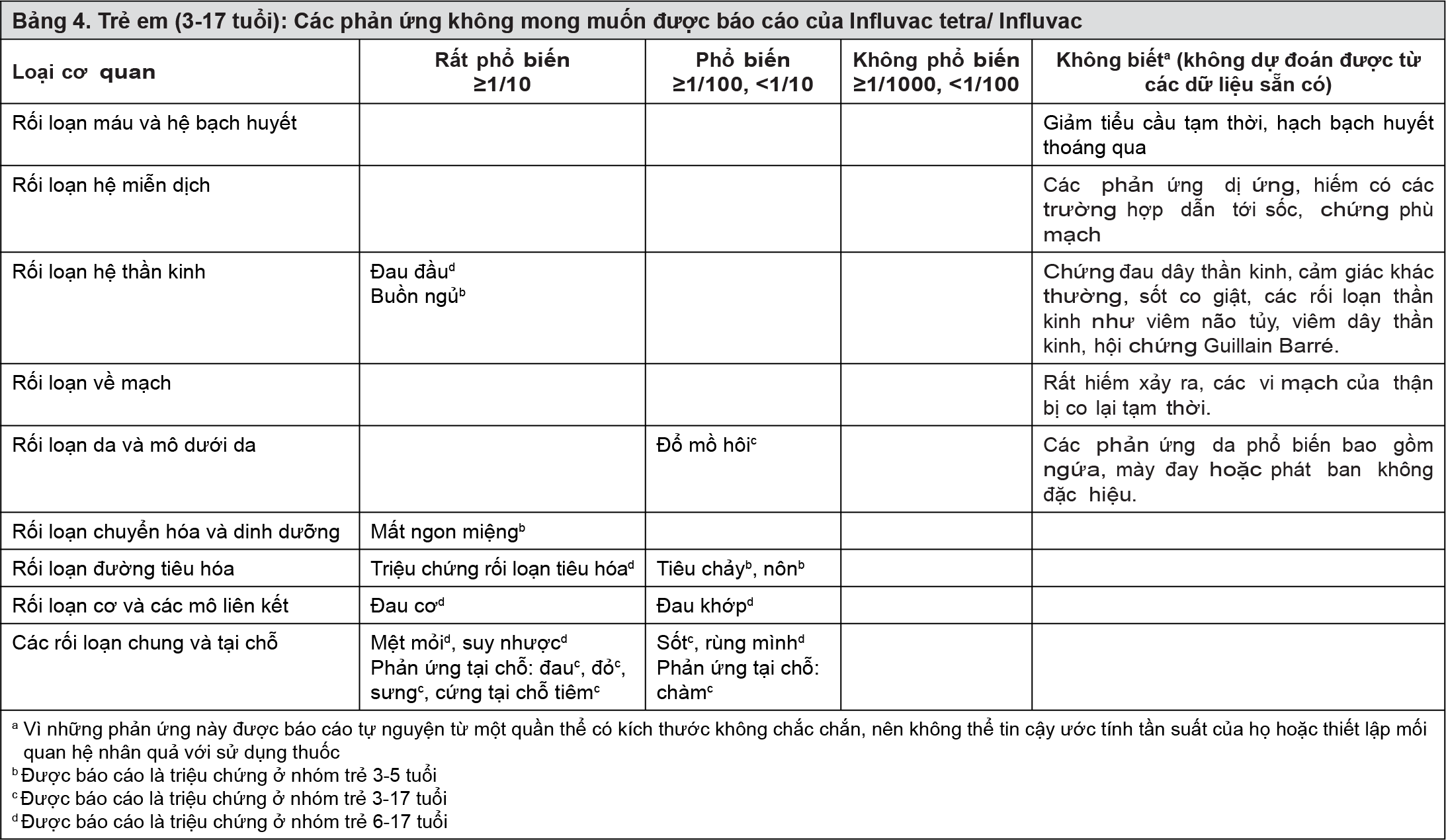
Trẻ em
- xem Bảng 4.
 Các tác dụng không mong muốn nghi ngờ được báo cáo
Các tác dụng không mong muốn nghi ngờ được báo cáo
Báo cáo tác dụng không mong muốn nghi ngờ sau khi thuốc được cấp phép rất quan trọng. Điều này cho phép tiếp tục theo dõi lợi ích/nguy cơ của các sản phẩm thuốc. Các chuyên gia y tế được yêu cầu báo cáo bất kỳ phản ứng phụ nghi ngờ thông qua hệ thống báo cáo an toàn tiêm chủng quốc gia Việt Nam.
Không chắc có bất kỳ một ảnh hưởng bất lợi nào khi dùng quá liều.
Các dấu hiệu cần lưu ý và khuyến cáo:
Vắc-xin phải được để đạt tới nhiệt độ phòng trước khi dùng.
Lắc trước khi dùng. Kiểm tra cảm quan trước khi dùng.
Vắc-xin không dùng và vật liệu thải loại khác phải được vứt bỏ theo đúng những quy định của địa phương về việc vứt bỏ các sản phẩm loại này.
Bảo quản ở nhiệt độ từ +2°C đến +8°C (trong tủ lạnh).
Không được đông băng.
Bảo quản trong bao bì gốc. Tránh ánh sáng.
Hạn dùng: 1 năm kể từ ngày sản xuất.
J07BB - Influenza vaccines ; Used for active immunizations.
Influvac Tetra Hỗn dịch tiêm
0.5 mL x 1's




 Đăng xuất
Đăng xuất





